-
USA - EnglishBrasil - Português
- Locais
- Acesso a SDS
- Início de sessão no CTVista®+
Por Brad Buecker, Ray Post, Jeremy Leitze e Mark Bush
Esse artigo examina os avanços no tratamento de água de recirculação aberta, incluindo uma mudança do tratamento de fosfato/fosfonato para a química de controle de corrosão e incrustação só com polímeros, seleção de biocidas oxidantes e não oxidantes para minimizar o depósito microbiológico e instrumentação analítica aprimorada para controle preciso de química de água de resfriamento.
A água de resfriamento é um produto fundamental na indústria do aço por causa da geração de muito calor e à transferência de energia em altos-fornos, fornos de arco elétrico e oxigênio básicos, processos de acabamento do aço etc. Muitos trocadores de calor dependem do resfriamento feito direta ou indiretamente pelos sistemas de recirculação, isto é, redes baseadas em torres de resfriamento. Incrustação, poluição microbiológica e corrosão nesses sistemas podem causar problemas sérios e podem até mesmo influenciar a produção da planta. Esse artigo examina os avanços e os desenvolvimentos mais recentes no tratamento de água de resfriamento de recirculação aberta, particularmente relacionados a corrosão e prevenção de incrustação. Esse artigo também examina uma tecnologia aprimorada de tratamento de água recuperada de processos de pulverização direta. A tecnologia pode oferecer uma economia significativa na planta.
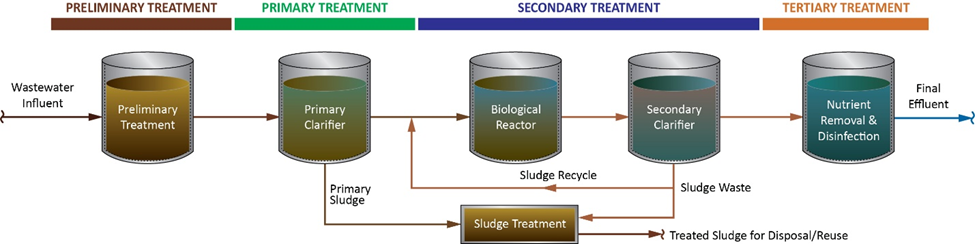
Impurezas e micro-organismos na água (e no ar que entra nas torres de resfriamento) influenciam a formação de incrustação, corrosão e lama por meio de uma variedade de mecanismos. Essas questões problemáticas frequentemente estão inter-relacionadas, como ilustrado na fig. 1.
Por exemplo, a formação de incrustação e a biodepósitos, além de limitarem a transferência de calor, podem induzir a corrosão sob depósito e a corrosão intersticial. A corrosão, por sua vez, pode gerar produtos que podem ser depositados em outro ponto, e assim por diante.
Como a fig. 1 indica, a corrosão, o biodepósito e a formação de incrustação podem ser influenciadas por outros fatores. Os métodos de tratamento para controle de incrustação e corrosão evoluíram, em grande parte, juntos, o que será tratado na seção a seguir. Para essa discussão, é importante uma breve revisão dos fundamentos básicos da corrosão.
Todos os mecanismos de corrosão são eletroquímicos por natureza, embora alguns, como a corrosão por erosão, sejam influenciados por fatores mecânicos. A Fig. 2 oferece um esquema do mecanismo de corrosão primário do aço carbono em água aerada.

O ferro é oxidado no ânodo e entra na solução como o íon ferroso (Fe+2). O processo libera elétrons que fluem através do metal para o cátodo, onde os elétrons reduzem o oxigênio dissolvido para íons hidroxila (OH-). Os íons de hidroxila reagem então com os íons de ferro solvatados para completar o circuito elétrico e formar um produto inicial de Fe(OH)2, que continua a oxidar para eventualmente formar ferrugem, com uma fórmula básica de Fe2O3∙xH2O. O ataque de oxigênio não controlado pode causar danos graves em redes de tubulação e também gerar depósitos que podem limitar parcial ou completamente o fluxo.
Também são possíveis outras reações catódicas. Uma das mais comuns é a corrosão em soluções ácidas, em que a reação catódica é:
Esse mecanismo de corrosão pode ser facilmente demonstrado em laboratório, colocando uma barra de ferro em uma solução de ácido clorídrico. Quase que imediatamente, bolhas de hidrogênio começam a aparecer enquanto o metal se desintegra rapidamente.
Inibidores de corrosão funcionam desacelerando as reações no anodo ou no catodo ou, às vezes, em ambos. Isso leva à discussão sobre um programa muito popular do século passado, que era de natureza simplista, mas fornecia bom controle de incrustação e corrosão. Questões ambientais exigiram que a técnica fosse abandonada, o que levou a uma mudança importante no método de tratamento, seguida pela evolução que está ocorrendo atualmente.
Nos anos que antecederam a década de 1970, o método mais comum para proteger o aço carbono era baseado na química de cromatos para proteção contra corrosão, com alimentação de ácido sulfúrico para controle de incrustação. O programa inibiu a incrustação de carbonato de cálcio (CaCO3) pela reação do ácido sulfúrico com íons de bicarbonato (HCO3-) para converter os íons em CO2, que escapa como gás e reduz a tendência de incrustação da solução. A Eq. 2 é representativa desta química:
Uma faixa de controle de pH típica estava entre 6,5 e 7,0. O segundo composto na formulação, o cromato dissódico (Na2Cr2O7), fornece íons de cromato
que reagem com o aço carbono para estabelecer uma camada protetora de aço pseudoinoxidável, particularmente na água de resfriamento saturada com oxigênio gerada pelas torres de resfriamento. Programas de cromato e ácido tinham um desempenho muito bom em muitas aplicações e o controle de químicos era bem simples.
Para trocadores de calor com tubos de liga de cobre, a química de azol complementar era e ainda é comum para proteger esses metais. Esse artigo não trata detalhadamente da química de azol, mas, resumindo, azóis são compostos orgânicos (um anel de benzeno no núcleo) com grupos funcionais de nitrogênio.
Os grupos de nitrogênio se ligam ao cobre, com os anéis parecidos com placas formando uma camada molecular na superfície do metal para protegê-lo do meio ambiente. Vários azóis, com vários grupos secundários, foram desenvolvidos para melhorar as propriedades de ligação e aumentar a resistência do azol contra degradação por outros produtos químicos, como biocidas oxidantes.
Uma maior compreensão da toxicidade do cromo hexavalente, em grande parte em resultado dos esforços de Erin Brockovich, levou à proibição da descarga de cromo no meio ambiente, o que basicamente eliminou o tratamento com cromato em sistemas de água de resfriamento abertos. O programa de substituição foi radicalmente diferente, com um conceito essencial sendo a operação com pH alcalino para ajudar no controle de corrosão.
O tratamento evoluiu rapidamente para uma química à base de fosfato para prevenção de incrustação e corrosão. Os programas normalmente funcionam com um pH moderadamente alcalino, o que minimiza a corrosão geral.
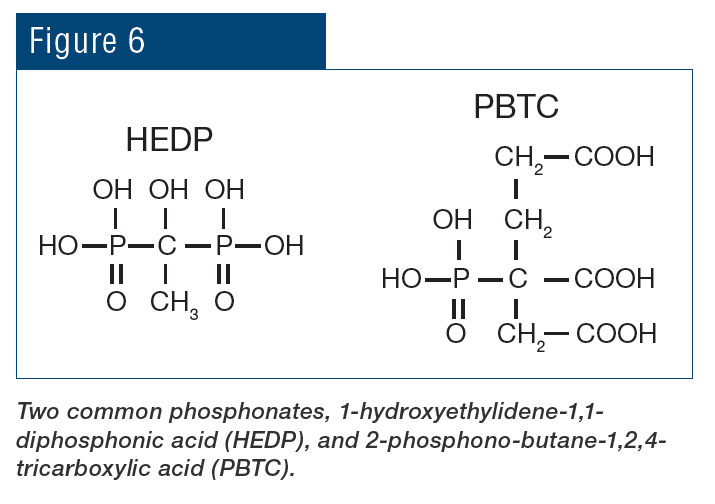

Além do aspecto do pH, a química também fornece proteção adicional contra corrosão, pois o fosfato reagirá com íons ferrosos (Fe+2) produzidos em locais anódicos para formar um depósito limitante da reação, enquanto o fosfato de cálcio [Ca3(PO4)2] precipita no ambiente alcalino local em locais catódicos para inibir a transferência de elétrons. No entanto, mesmo pequenos transtornos nos programas de fosfato podem causar incrustação grave de fosfato de cálcio e, em um momento, o excesso de depósito de Ca3(PO4)2 tornou-se quase tão grande quanto o problema que a incrustação de carbonato de cálcio tinha sido antes. Assim sendo, os métodos de tratamento evoluíram para metodologias mais tolerantes e, em muitos casos, a espinha dorsal desses programas são os fosfatos orgânicos (fosfonatos).
Os fosfonatos se ligam aos depósitos à medida que se formam e inibem o crescimento de cristais e a força do seu entrelaçamento.
Um programa comum de tratamento com fosfato/fosfonato pode incluir um ou talvez dois dos compostos fosfonatos em dosagens baixas de mg/L para controle de incrustação primária, 5–15 mg/L ou mais de ortofosfato para controle de incrustação adicional e proteção contra corrosão e talvez 0,5–2,5 mg/L de zinco. O zinco reage com os íons hidroxila gerados nos cátodos para formar um precipitado [Zn(OH)2], que fornece proteção catódica adicional. (Também é importante observar que a descarga de zinco está sujeita a regulamentos mais rigorosos.) Tipicamente incluídos nessas formulações estão 5–10 mg/L de polímero orgânico para controle da deposição de fosfato de cálcio.
Os programas de fosfato/fosfonato estão longe de serem simples, e alimentação em excesso ou abaixo do ideal pode resultar em corrosão ou formação de incrustação. Mesmo com a química aparentemente adequada, os depósitos de inibição de corrosão são porosos, e também podem ser lavados. Quanto a preocupações ambientais, a descarga de fósforo apresenta problemas cada vez mais difíceis.
O fósforo, juntamente com o nitrogênio e o carbono, é um macronutriente essencial para todas as formas de vida. Algas derivam suas exigências de carbono do bicarbonato e do carbonato inorgânicos utilizando a energia da luz solar para converter o carbono inorgânico em carbono orgânico para crescimento de tecido celular. Algumas espécies de algas também são capazes de “corrigir” o gás nitrogênio atmosférico
usando a enzima nitrogenase para converter N2 em amônia e outros compostos necessários para a biossíntese de ácidos nucleicos e proteínas. Comum entre as espécies de correção de nitrogênio fossintéticas estão as cianobactérias, comumente chamadas de “algas azuis”. Os fósforo é frequentemente o nutriente limitador do crescimento em sistemas aquáticos, pois está presente em concentrações relativas muito baixas em comparação com as exigidas pelas plantas.
As cianobactérias são conhecidas por sua florações amplas e altamente visíveis. A Fig. 8 mostra uma fotografia aérea de uma cianobactéria florescendo na bacia rasa ocidental do Lago Erie em 2011.

O crescimento indesejável e esteticamente desagradável de algas no Lago Erie resultou em praias sujas, redução do turismo e uma queda das populações de peixes. Além do impacto sensorial nocivo, as cianobactérias também podem produzir microcistinase e outras cianotoxinas que são tóxicas para peixes, pássaros e mamíferos. Muitos leitores têm conhecimento de grandes florações de algas tóxicas em outros locais, mais notadamente na Flórida.
A química de fosfato/fosfonato também oferece um nutriente essencial, o fósforo, para crescimento microbiológico em torres de resfriamento, particularmente, de algas.
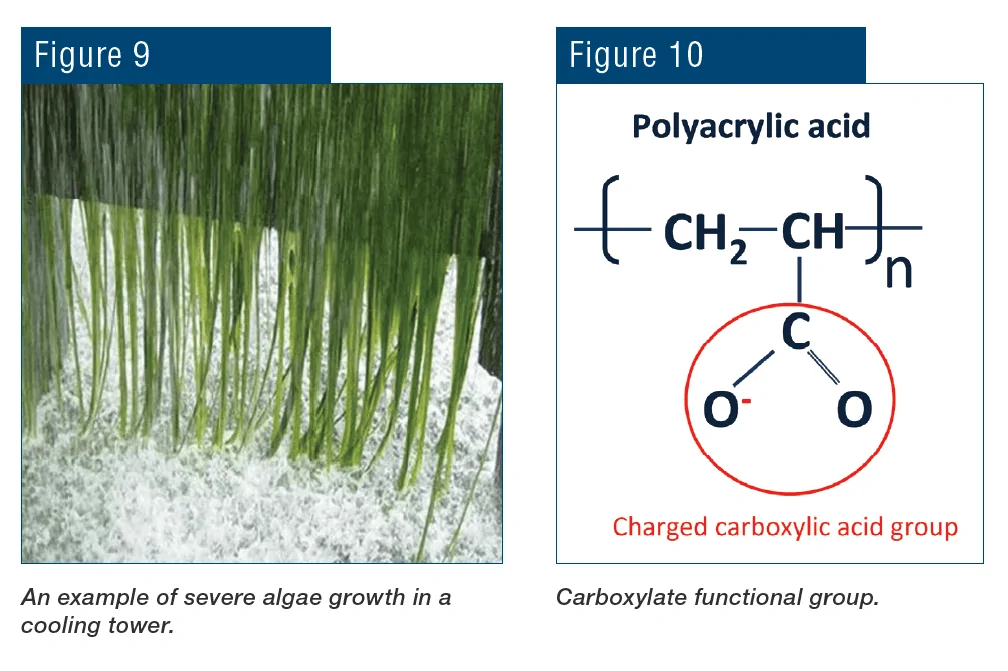
O controle de algas adequado pode exigir uma alimentação substancial de microbiocidas, que podem aumentar grandemente o custo de tratamento da água de resfriamento.
Esses problemas estão levando a uma nova evolução: o tratamento de água de resfriamento com polímeros e sem componentes de fósforo (e frequentemente sem zinco). Aplicações bem-sucedidas para controle de incrustação são conhecidas há muito tempo, mas novos materiais para a inibição de corrosão estão se provando bem-sucedidos, incluindo em siderúrgicas.
As formulações de polímeros contendo o grupo carboxilato foram utilizadas com sucesso por décadas para controlar a incrustação de carbonato de cálcio (CaCO3) em água de resfriamento.
Contudo, muitos outros depósitos são possíveis, incluindo os silicatos de cálcio e magnésio, sulfato de cálcio, fluoreto de cálcio e dióxido de manganês, para mencionar alguns dos mais comuns. A necessidade de combater esses
e outros formadores de escala geraram desenvolvimento de copolímeros e terpolímeros, contendo grupos funcionais alternativos ou suplementares, incluindo sulfonatos (SO3-), acrilamida (H2N-C-O) e outros. Os polímeros inibem a formação de incrustação por meio de dois mecanismos: sequestro de íons e modificação de cristais.
Porém, uma pergunta muito importante permanece: “Qual a eficácia de uma programa sem fosfato/fosfonato para inibição de corrosão?" Em primeiro lugar, os tratamentos não P foram projetados para operar em uma faixa de pH alcalino (7–9), que tende a minimizar a corrosão geral de metais. Mesmo assim, as células de corrosão ainda conseguem se desenvolver em um ambiente alcalino. A chave é que o inibidor de corrosão estabelece uma barreira protetora direta em superfícies de metal. Um produto que surgiu, o FlexPro®, combina um grupo de químicas que “interagem diretamente com superfícies de metais para formar um complexo inibidor de amido poli-hidroxi reativo (reactive polyhydroxy starch inhibitor, RPSI) que é independente de cálcio, pH ou outros componentes químicos para água”.1
A aplicação em escala total desse produto químico se provou muito eficaz. Em um caso, em um grande complexo industrial no sudeste dos EUA, o RPSI substituiu os produtos químicos anteriores à base de polifosfato e, depois, de zinco. As taxas de corrosão do aço carbono foram reduzidas de 0,20 para 0,25 mm/ano para 0,0025 para 0,0075 mm/ano. Em uma observação secundária, a mudança de zinco para RPSI foi influenciada, em parte, por problemas com grave formação de algas em um tanque de clarificação e reciclagem na planta. A remoção de fosfato da água resolveu essa dificuldade.
Em outro exemplo, em uma grande planta química na Costa do Golfo, o tratamento químico tradicional com fosfato se provou satisfatório para controle de corrosão, mas depósitos de fosfato de cálcio causaram incrustação em alguns dos trocadores de calor de placas da planta. Esses trocadores são conhecidos por serem locais de baixo fluxo e acúmulo de depósito. A migração para o tratamento com RPSI manteve a excelente proteção contra corrosão e eliminou o depósito de fosfato.

As químicas e as tecnologias de tratamento de água mencionadas neste artigo são adequadas para muitas aplicações industriais, conforme descrito no exemplo a seguir de uma unidade de laminação da SSAB.
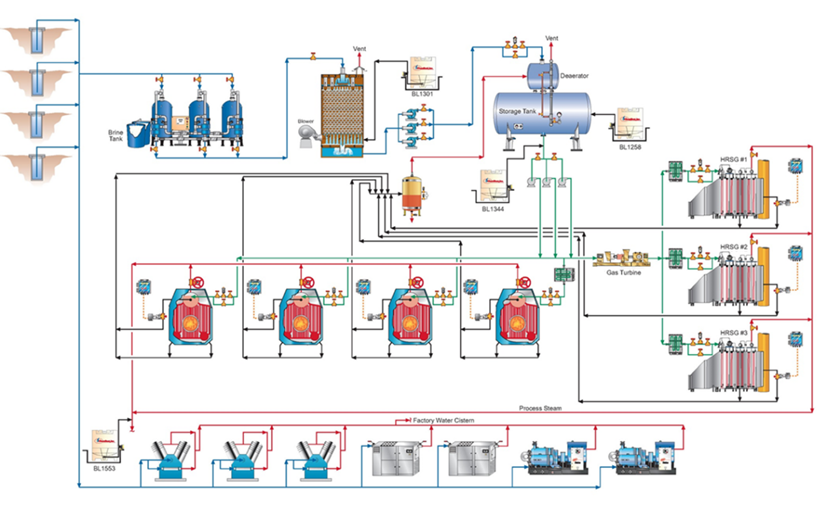
Na usina da SSAB em Mobile, Alabama, Estados Unidos, o FlexPro foi aplicado ao sistema de resfriamento sem contato e ao sistema de resfriamento por pulverização de contato direto da usina de laminação a quente. A Fig. 12 ilustra a redução na taxa de corrosão após a mudança da química de fosfato para a química de RPSI.
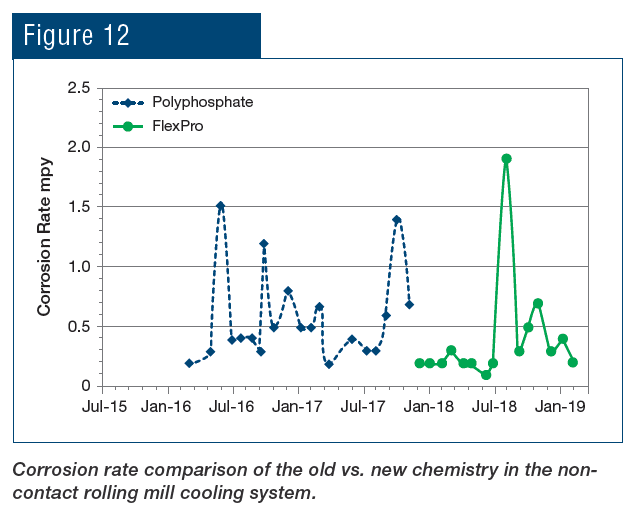
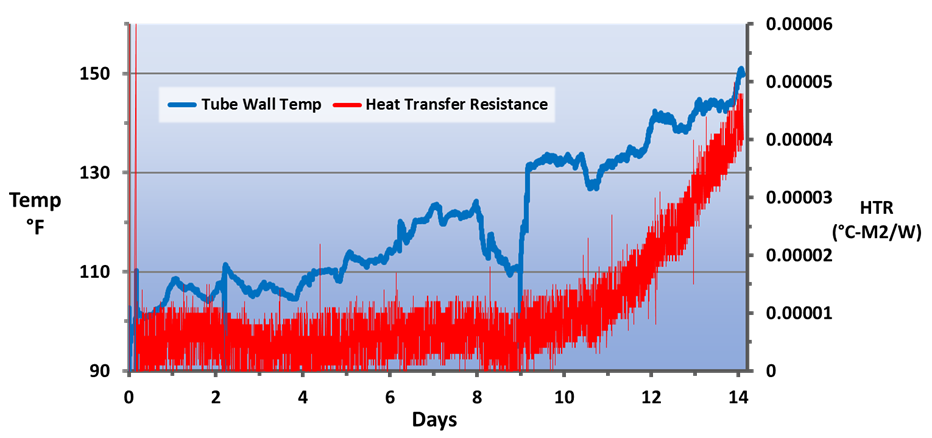
Como pode ser visto, não houve apenas redução da taxa de corrosão, mas o controle se tornou mais estável após a introdução da química de polímero. Resultados ainda mais pronunciados foram alcançados no sistema de resfriamento por água de serviço (Fig. 13).
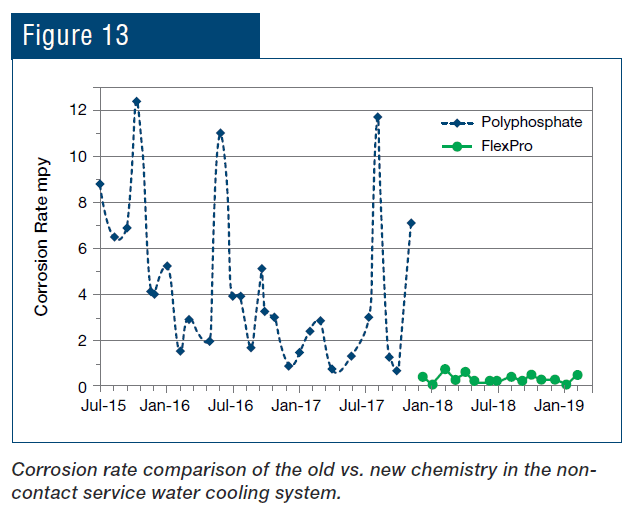
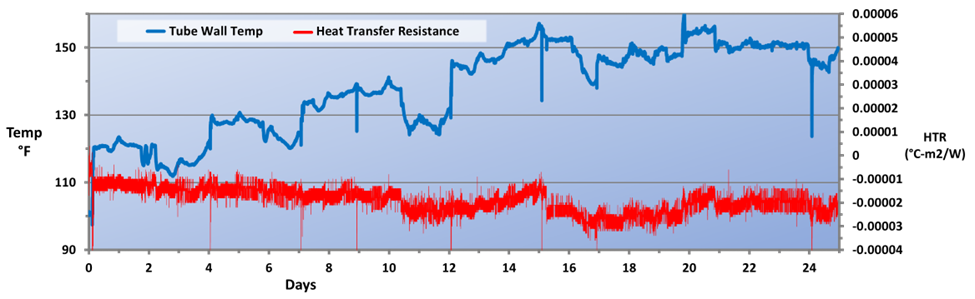
Uma aplicação que é exclusiva das usinas de laminação, diferente de muitas outras indústrias, é a proteção de metais resfriados por pulverizações diretas. O tratamento RPSI foi implementado no laminador de tiras a quente da planta por mais de um ano, com resultados mostrados na Fig. 14.
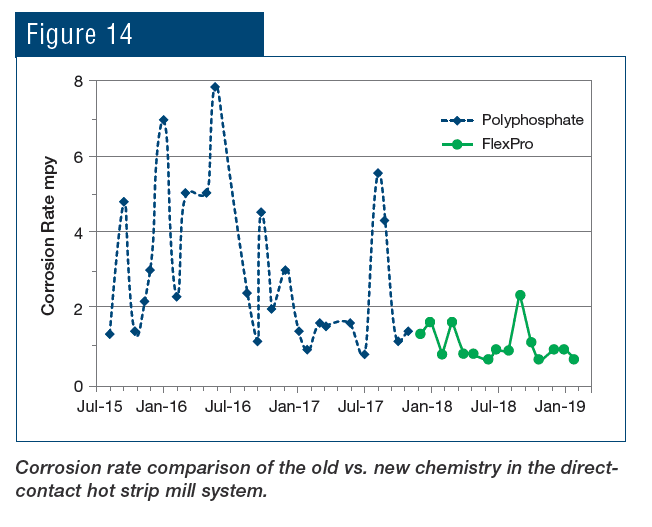
Para enfatizar novamente, o mais importante é que a química estabelece uma camada protetora direta no aço em vez de depender da precipitação de compostos de fosfatos para inibir a corrosão. A mudança no tipo de química forneceu os seguintes benefícios à planta:
Aprimoramentos no tratamento de água de resfriamento continuam a beneficiar muitas indústrias, e uma das mais importantes é a indústria do aço. Os proprietários, operadores e equipes técnicas de usinas agora têm acesso a ferramentas novas e aprimoradas para reduzir a corrosão e a incrustação, não apenas em sistemas de água sem contato, mas também em aplicações de pulverização direta. Os aprimoramentos podem economizar custos significativos das plantas, por meio da proteção da infraestrutura e da maior confiabilidade do equipamento. As pesquisas e testes continuam, em relação a outras possíveis melhorias de processo.
Os resultados são apenas exemplos. Não são garantidos. Os resultados reais podem variar.
2020 pela AIST. Distribuído com permissão da AIST. Todos os outros tipos de distribuição são proibidos.
