Por Katie Perryman, Ed Sylvester e Brad Buecker, ChemTreat, Inc.
Este artigo apareceu originalmente no The Analyst, uma publicação da AWT .
A água com alta pureza costuma ser essencial para geradores de vapor que produzem energia, uma vez que condições de alta temperatura/pressão exigem controle das impurezas para concentrações de partes por bilhão (ppb) baixas para evitar corrosão grave e poluição. Entretanto, para as milhares de caldeiras de baixa pressão em plantas industriais ao redor do país, as exigências de pureza de água geralmente não são rígidas. Contudo, incidentes onde um projeto inadequado ou falhas no sistema de tratamento de água de reposição induziram à corrosão e incrustação severas têm sido relatados há décadas e continuam a ocorrer. Isso pode levar à perda de produção e a reparos ou substituições caros de equipamento. Este artigo apresenta uma perspectiva sobre a importância do tratamento de água de reposição para caldeiras de baixa pressão e descreve as tecnologias modernas para produção de água de reposição de boa qualidade com custo razoável.
Geradores de vapor de baixa pressão
O vapor de baixa pressão (pressões abaixo de 900 libras por polegada quadrada [psig] em geral e frequentemente entre 50 e 600 psig) é usado em muitas plantas industriais pelo país. Por exemplo, o vapor geralmente serve para diversos processos em refinarias, incluindo como fonte de calor integral no processo de destilação atmosférica e nos processos de craqueamento e reforma. O vapor alimenta turbinas para a produção de ar nos altos-fornos nas siderúrgicas; nos digestores e concentradores nas fábricas de papel; evaporadores, cristalizadores e tanques de reação nas indústrias químicas; e sistemas de aquecimento de edifícios em todos os lugares. A lista continua.
O estímulo para este artigo vem da experiência direta dos autores e relatórios muito frequentes dos nossos colegas que, ao entrar nas plantas pela primeira vez, encontram geradores de vapor com incrustações, corrosão sérias ou problemas de pureza do vapor que podem ser diretamente rastreados de volta ao projeto inadequado ou atenção inadequada ao sistema de água de reposição (e frequentemente, aos produtos químicos do retorno de condensado). Isso frequentemente parece ocorrer como resultado do gerenciamento da planta, operadores ou equipe técnica que focam nos produtos químicos do processo e na engenharia, com geração de vapor (e sistemas de água de resfriamento) aparecendo como entidades nebulosas que exigem menos atenção.
A maioria das caldeiras em grandes plantas industriais é do estilo tubo de água, frequentemente do tipo pacote, embora caldeiras grandes possam ser erguidas em campo. As taxas de vapor (libras por hora [lb/h]) costumam ser na faixa de cinco a seis dígitos. É comum que essas caldeiras incluam superaquecedores para aumentar a temperatura do vapor acima do ponto de saturação e garantir que o vapor tenha a energia correta e/ou permaneça seco até o ponto de uso. Para caldeiras que alimentam turbinas, superaquecimento é exigido para evitar a condensação excessiva na turbina, o que poderia danificar as pás.
Problemas com o tratamento da água de reposição
Provavelmente, desde o tempo em que os seres humanos começaram a esquentar água para as necessidades pessoais, nossa espécie tem observado depósitos nos tanques aquecidos. Esses problemas se tornaram mais graves depois da invenção e do uso expandido de motores a vapor durante a Revolução Industrial dos séculos 18 e 19. O principal culpado foi (e frequentemente ainda é) o depósito de carbonato de cálcio.
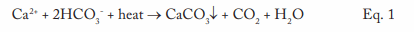
Esta equação descreve a reação dos íons de cálcio (Ca2+) e a alcalinidade do bicarbonato (HCO3–) que podem ocorrer em sistemas de água quente e caldeiras. Um ponto crítico a observar é que o CaCO3 é um sal inversamente solúvel, cujo potencial de deposição aumenta conforme o aumento de temperatura. Como claramente ilustrado na Figura 1, não se trata de um mecanismo que tem sido relegado ao passado.

À medida que geradores de vapor aumentaram a capacidade de pressão e potência no último século, métodos para minimizar e controlar a incrustação de CaCO3 se tornaram necessários. Uma solução comum da década de 30 em diante tem sido o abrandamento da água de reposição com zeólito de sódio, uma tecnologia que se tornou prática com o desenvolvimento das resinas de troca de íons sintéticas (Figura 2).

Cada um desses leitos contém bilhões de locais ativos que, para abrandamento do sódio, geralmente são grupos de ácidos sulfônicos com sódio ligado (SO3–Na+). A figura 3 ilustra uma configuração básica de um tanque de abrandamento.
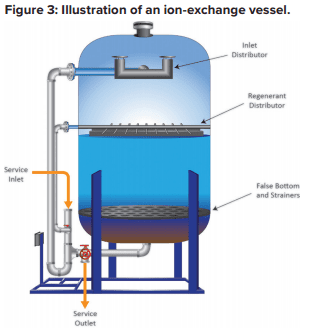
À medida que a água de reposição passa pelo tanque, o cálcio (Ca2+) e o magnésio(Mg2+) são trocados por sódio. A afinidade mais forte é pelo cálcio, seguida pelo magnésio, de modo que conforme o serviço progride, a resina desenvolve camadas estratificadas.

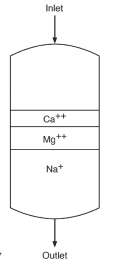
O fluxo abrandado, com a dureza removida, ainda contém outros íons dissolvidos, incluindo alcalinidade, cloreto (Cl–), sulfato (SO42-) e sílica (SiO2). Quando o leito atinge a exaustão, ele é regenerado com uma solução de salmoura que leva os íons de dureza para um fluxo de resíduos, que é descartado.
Nesse ponto, diversas características do abrandamento de sódio exigem alguma discussão extra. Muitos sistemas de geração de vapor de baixa pressão foram projetados com o abrandamento de sódio como o principal método de tratamento da água de reposição, sem mais nenhum tratamento adicional. E, na verdade, isso pode ser suficiente para diversos geradores de vapor. A Tabela A descreve algumas diretrizes gerais, extraídas da conceituada Sociedade Americana de Engenheiros Mecânicos (American Society of Mechanical Engineers, ASME), relacionadas aos limites de impureza nas caldeiras industriais estilo tubo, de baixa a média pressão.
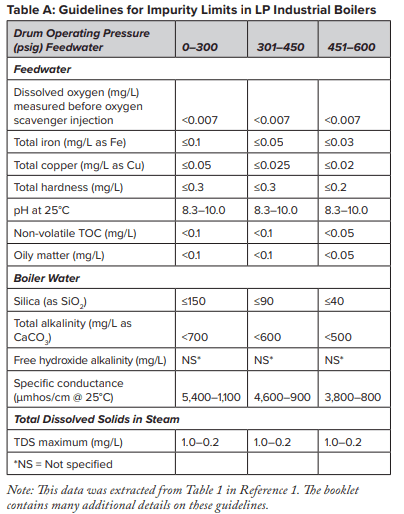
Os dados indicam que uma quantidade significativa de alcalinidade pode ser tolerada nas caldeiras de baixa pressão e, para a maioria das aplicações, um pouco de alcalinidade é desejada, uma vez que ela protege superfícies metálicas contra corrosão, um ponto no qual retornaremos mais tarde. Entretanto, o HCO3, ao atingir a caldeira, é, em grande parte convertido em CO2 por meio das seguintes reações nas Equações 2 a 4.
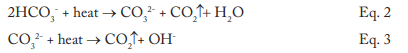
A conversão para dióxido de carbono (CO2) das reações combinadas pode chegar a 90%. O CO2 sai com o vapor, e quando o CO2 é dissolvido novamente no condensado, isso pode aumentar a acidez do retorno de condensado.
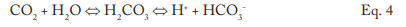
Embora o pH gerado por essa reação tenha um limite inferior relativamente moderado, é mais do que suficiente para causar corrosão significativa do aço carbono nos sistemas de retorno de condensado. Por exemplo, 3 partes por milhão (ppm) de CO2 em condensado de vapor puro reduzirão o pH para 5,26. Se o oxigênio dissolvido estiver presente no sistema, a corrosão pode ser consideravelmente amplificada.
A operação da unidade que pode minimizar a produção de CO2 no gerador de vapor é ilustrada no diagrama fundamental a seguir.
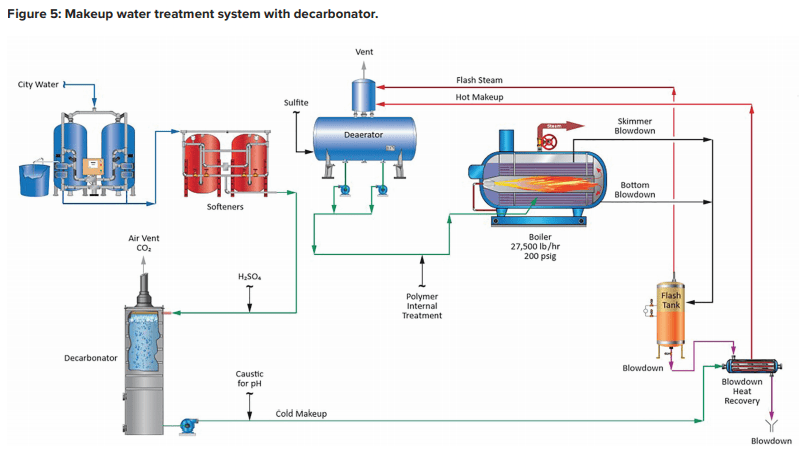
Observe a inclusão de um descarbonador de ventilação forçada com injeção de ácido na alimentação. A equação 4 das forças de condicionamento do ácido à esquerda e um descarbonador bem projetado podem reduzir a concentração de CO2 para um nível baixo de partes por milhão (ppm). O fluxo a jusante de alimentação da soda cáustica do descarbonador então eleva o pH da água até torná-la menos corrosiva em seu percurso até a caldeira. Observação: Se a atemperação do vapor for fornecida por injeção direta de água de alimentação do desaerador, então a soda cáustica não poderá ser usada para elevar o pH. Um composto não volátil (por exemplo, amônia, amina) é necessário.
Outro problema brevemente mencionado acima agora exige um pouco de discussão. Frequentemente, quando representantes técnicos começam a visitar uma planta pela primeira vez, eles encontram caldeiras com depósito de incrustação, corrosão ou ambos. Em muitos casos, a equipe da planta revelará problemas com o amaciante que levaram aos avanços na dureza. A equação 1 e a Figura 2 ilustram os possíveis efeitos de tais dificuldades. Mas até mesmo um amaciador/descarbonizador operando corretamente ainda permite que muitos íons como cloreto e sulfato entrem na caldeira. Sem uma atenção especial aos produtos químicos da água da caldeira e o controle de purga da caldeira, o acúmulo desses íons pode causar corrosão e outros problemas, incluindo a formação de espuma nos tambores da caldeira. Isso, por sua vez, pode levar à contaminação do vapor e a problemas a jusante. Para enfatizar novamente, o sistema de reposição do gerador de vapor e o controle dos produtos químicos da água da caldeira exigem tanta atenção quanto as operações do processo.
Algo melhor do que amaciante?
Para sistemas de reposição modernos, a osmose reversa (RO) oferece uma alternativa confiável para o amaciamento, onde até mesmo os sistemas básicos podem remover mais de 99% de todos os íons da água. O processo de osmose é conhecido há anos. Duas soluções de concentrações diferentes, quando separadas por uma membrana semipermeável que permite apenas a passagem de água, induzirá a água na solução diluída a se mover através da membrana para a outra solução para equilibrar a concentração. Esse fenômeno induz à uma pressão osmótica na membrana até que as soluções alcancem o equilíbrio. Como o nome osmose reversa diz, a reação é operada no inverso e a pressão produz água purificada a partir de um fluxo mais concentrado.
A possível aplicação da osmose reversa como método de tratamento de água de reposição se tornou bem conhecida no último século e se popularizou com o desenvolvimento e as melhorias da tecnologia de membrana em espiral.
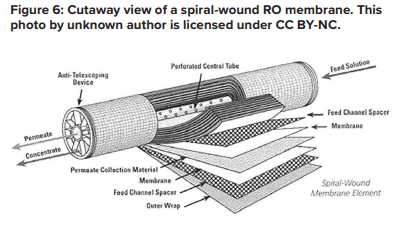
Uma membrana lisa possui diversas camadas como uma espinha dorsal, que são todas enroladas ao redor de um núcleo de plástico central perfurado. A alimentação entra pela extremidade dianteira de cada elemento e flui ao longo do transportador de água de alimentação enquanto a pressão empurra a água pela membrana. A água purificada, conhecida como permeado, flui até o núcleo central, e a água de alimentação cada vez mais concentrada (resíduo) sai do elemento.
Cada tanque de pressão da osmose reversa geralmente possui diversos elementos em uma série.
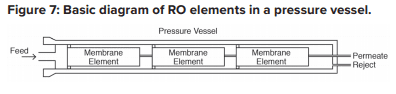
Anéis em “O” vedam cada elemento ao longo das paredes do tanque de pressão de modo que a água de alimentação não provoque curto-circuito de nenhum elemento. Um tanque de pressão de osmose reversa típico terá cinco ou seis elementos.
A configuração é projetada para processar a água através de um mecanismo conhecido como clarificação tangencial.
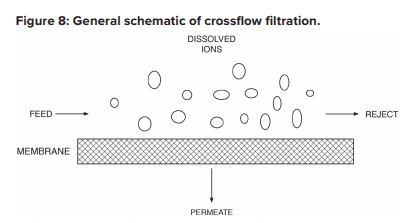
A alimentação flui paralela às membranas da osmose reversa e a pressão força a água pura pelas membranas, enquanto as impurezas são transportadas para longe com o rejeito. Somente alguns íons monovalentes menores (Na+, Cl-, sílica, HCO3) passa pelas membranas. Entretanto, embora a clarificação tangencial tenha sido projetada para manter impurezas suspensas no vapor residual, é inevitável que até mesmo com reposição excepcionalmente limpa, os compostos irão gradualmente se acumular nas superfícies da membrana. Em geral, sólidos residuais suspensos que não são capturados pelo pré-tratamento vão se acumular nas principais membranas do sistema de osmose reversa. Inversamente, por causa do concentrado de íons dissolvidos enquanto a água passa de uma membrana para a próxima, a incrustação se torna uma preocupação cada vez maior nos elementos a jusante.
O sistema básico de osmose reversa é do tipo passagem única com dois estágios, conforme descrito na Figura 9.
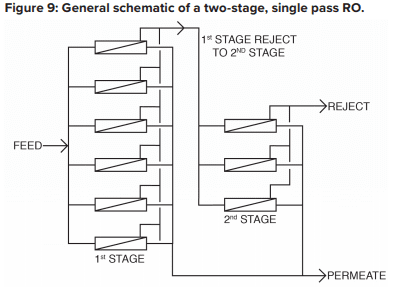
Uma característica crítica da osmose reversa está ilustrada neste diagrama. Com águas de alimentação “normais”, aproximadamente 50% da água de alimentação é convertida em permeado em cada tanque de pressão de primeiro estágio. Isso significa que sem processamento posterior, 50% da água de alimentação seria desperdiçada. No modelo de dois estágios mostrado acima, a água de alimentação bruta flui por seis tanques de pressão paralelos no primeiro estágio, e o rejeito desses tanques é direcionado por três vasos de pressão adicionais no segundo estágio. A recuperação total de água aumenta para 75%.
Em algumas aplicações, especialmente aquelas para produção de água com pureza ultra-alta, a osmose reversa de passada dupla é comum. Nessa configuração, o permeado da primeira passada é tratado em um conjunto separado de membranas. Uma vez que a água de alimentação já foi significativamente purificada, 85% a 90% da recuperação da segunda passada é alcançável. O rejeito é reciclado de volta à entrada da primeira passada e nenhuma água é descarregada como residual da segunda passada.
A osmose reversa se tornou muito popular em diversas aplicações nos últimos anos, especialmente para unidades que geram energia à base de vapor. A osmose reversa mais os trocadores de íons de leito misto de polimento ou eletrodeionização podem produzir água com alta pureza necessária para a geração de vapor.
Controle de incrustação e poluição na osmose reversa
As membranas da osmose reversa, especialmente os elementos principais, estão sujeitas à poluição por partículas. Uma medição importante para determinar o potenncial dessa poluição é o índice de densidade de silte (silt density index, SDI). Geralmente, filtros com profundidade de 5 micra (µm) são instalados à frente da osmose reversa para minimizar a possibilidade de poluição por partículas. Os testes de SDI devem ser realizados no efluente desses filtros. O teste de SDI é simples. Uma amostra fluída da água de alimentação da osmose reversa, a jusante dos filtros de cartucho, é direcionada através de um filtro de 0,45 µm a uma pressão de 30 psig. A medição é tomada do tempo para que 500 mililitros (ml) de água passem pelo filtro no início do teste (ti) e novamente depois de 15 minutos (tf). O SDI é calculado conforme mostrado na equação 5:

Uma regra geral é que o SDI deve ficar pelo menos abaixo de 5 e, de preferência, abaixo de 3. Entretanto, o SDI não deve ser o único critério que determina a adequação de uma aplicação de osmose reversa. O tipo de água e/ou a natureza dos contaminantes também devem ser considerados. Por exemplo, em uma aplicação, as leituras de SDI da alimentação da osmose reversa sempre ficou entre 1 e 3. Ainda assim, as membranas estavam sujas com partículas de óxido de ferro excepcionalmente finas.
A formação de incrustação é outro problema que exige atenção. Quando a água flui pelo tanque de pressão de osmose reversa, o concentrado acumula continuamente os sólidos dissolvidos, o que aumenta a possibilidade de incrustação. Carbonato de cálcio e sulfato de cálcio podem se acumular até um ponto onde a precipitação começa a ocorrer. Outros depósitos possíveis incluem sílica e silicatos metálicos alcalinos, sulfato de estrôncio, sulfato de bário e fluoreto de cálcio. Embora o pré-tratamento possa reduzir as concentrações de muitos compostos formadores de incrustações, o restante ainda pode causar problemas. Incrustações de sulfato de bário e de estrôncio são especialmente difíceis de remover. Fabricantes de membranas conceituados desenvolveram programas para calcular os limites de solubilidade desses sais. O programa avisará ao usuário se qualquer limite de solubilidade for excedido. Os programas também fornecem cálculos de “normalização” do sistema de osmose reversa, conforme descrito adiante.
A alimentação de anti-incrustante é comum em sistemas de osmose reversa. Anti-incrustantes comuns incluem poliacrilatos e fosfonatos. Anti-incrustante ou mistura corretos podem controlar sulfato de cálcio em um fator de 7 acima do limite de saturação, o sulfato de estrôncio 800% acima do limite de saturação e o sulfato de bário 6.000% acima do limite de saturação.
Produtos químicos pré-tratamento podem afetar o desempenho da membrana. Os agentes de coagulação da variedade catiônica e, mais notadamente, os compostos de alumínio e alguns coagulantes orgânicos/floculantes são especialmente problemáticos para as membranas de osmose reversa. Se esses agentes estiverem presentes, deve-se considerar métodos para removê-los. Geralmente introduzido como alvejante e injetado na reposição da planta primária para controlar a incrustação microbiológica, cloro reagirá com os átomos de nitrogênio nas membranas de osmose reversa e danificará irreversivelmente os materiais. O cloro deve ser removido a montante da osmose reversa, mas a ausência de biocidas deixa as membranas em risco de ataque microbiano. A figura 10 mostra como bioincrustação pode danificar um elemento da membrana.

Bioincrustação pode provocar dano irreversível às membranas, uma vez que os depósitos não podem ser completamente removidos por métodos de limpeza padrão. É essencial minimizar condições que podem levar a depósitos microbiológicos. Técnicas alternativas ao cloro estão disponíveis para minimizar o depósito de micróbios dentro das membranas. Uma é o tratamento periódico com biocida sem oxidação ou com oxidação moderada (a frequência depende no potencial de poluição). Uma escolha popular é o dibromo-nitrilo-propionamida (DBNPA). O diagrama do produto químico DBNPA é mostrado na Figura 11.
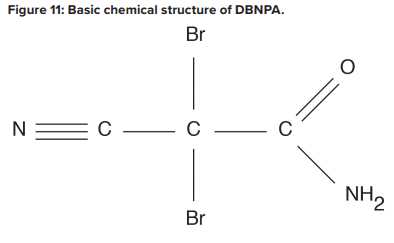
O DBNPA é um biocida de ação rápida que pode ser prontamente removido de qualquer descarga ao elevar o pH até cerca de 9, ou comumente tratado com bissulfito de sódio. Outra possibilidade é uma versão especializada do dióxido de cloro (ClO2).A Esse produto pode soar surpreendente, uma vez que dióxido de cloro pode agir como um oxidante forte nas aplicações de água de resfriamento. Entretanto, nesse caso, o cloro não está livre e assim, não reage com os átomos de nitrogênio nas membranas.
Limpeza da osmose reversa
Mesmo com pré-tratamento bem controlado e produtos químicos anti-incrustação, as membranas de osmose reversa ainda coletarão depósitos. Os principais elementos reúnem sólidos suspensos e coloidais residuais, enquanto os elementos a jusante, especialmente aqueles no segundo estágio, apresentam concentrações mais altas de íons dissolvidos que podem se precipitar. Além disso, o problema é que a pressão exigida para empurrar a água através das membranas pode reter algumas dessas partículas no lugar. Se o acúmulo de impurezas não for inspecionado, o eventual resultado é a poluição irreversível da membrana.
Portanto, programas de normalização são essenciais para determinar a necessidade e o agendamento de limpezas de RO. A temperatura tem um impacto significativo no fluxo e na pressão do permeado, e as mudanças de temperatura podem mascarar variações de fluxo e pressão causadas pelos sólidos suspensos ou acúmulo de incrustação. Programas de normalização usam medições de temperatura, pressão e fluxo para fornecer valores corrigidos para todas as condições de temperatura. Uma regra útil é programar limpeza quando o valor normalizado tiver caído 10% a 15% da linha de base. Programas de normalização também podem ajudar a detectar um aumento na passagem de sal causado por uma membrana com defeito ou degradada, que poderia, de outro modo, ser atribuído aos efeitos da temperatura.
Um processo de limpeza de duas etapas frequentemente é empregado para possivelmente remover uma ampla variedade de incrustantes que podem se acumular nas membranas de osmose reversa. Geralmente, na primeira etapa, uma solução com pH alto (12 a 35 °C) é circulada pelas membranas. A solução alcalina remove os compostos orgânicos, microbiológicos e outros que possam ter se acumulado. Esse estágio é seguido por uma lavagem e, frequentemente, um estágio com pH baixo de ácido cítrico como principal ingrediente. O pH baixo ajuda a remover os sais minerais solúveis como, por exemplo, carbonato de cálcio, enquanto o ácido cítrico causa quelação com metais, em sua maioria, ferro. A inclusão de um aquecedor no ciclo de limpeza pode acelerar significativamente o processo.
Um conceito importante é limpar cada estágio separadamente. Do contrário, as impurezas extraídas de um estágio podem sujar o outro e vice-versa. Também, os sistemas de limpeza são geralmente projetados com filtros de cartucho no ciclo de limpeza para coletar sólidos durante o processo. Esses filtros devem ser substituídos após cada etapa na limpeza.
O anterior é apenas uma orientação geral. Consulte seu fabricante de membranas de osmose reversa para orientação específica.
Problemas com o fluxo de resíduos da osmose reversa.
Conforme observado, um sistema de osmose reserva típico de dois estágios e passagem única recupera aproximadamente 75% da alimentação de entrada e produz um fluxo residual (rejeito) dos 25% restantes. Esse fluxo precisa ser descartado em algum lugar. Em plantas com torres de resfriamento, a bacia de uma das torres frequentemente é o local ideal para os resíduos. Alternativamente, muitas plantas têm instalações de tratamento de águas residuais para tratar água de descarga antes de liberá-la ao meio ambiente. O resíduo da osmose reversa é praticamente o concentrado de reposição da planta por um fator de quatro, então ele não deve sobrecarregar o equipamento de tratamento de águas residuais.
Problemas com o tratamento de água de reposição relacionados ao tratamento de água de caldeira
Diversos programas de tratamento estão disponíveis para caldeiras de baixa pressão, que podem incluir fosfatos, polímeros orgânicos e, algumas vezes, agentes quelantes. Tais programas devem ser feitos sob medida para os produtos químicos da água que entra na caldeira pela fonte de reposição e de retorno de condensado. Uma alteração na água abrandada para permeado de osmose reversa pode impactar significativamente no tratamento de água de caldeira e até mesmo no tratamento da água de alimentação. Águas com maior pureza são frequentemente conhecidas como água “pura” porque a falta de íons dissolvidos faz com que metais cedam íons para a água. Embora os íons de bicarbonato não possam reagir com cálcio para formar incrustação, em muitos casos, eles formarão uma camada de proteção solta nos metais. Para a equipe da planta que considera uma mudança da água abrandada para osmose reversa, esses e outros fatores devem ser considerados antes de fazer a mudança. E, considerando que as caldeiras devam ter um influxo menor de dureza, o programa de tratamento poderá precisar de modificação para dar conta dessa alteração química. Um fator de extrema importância em muitas plantas é a proporção de água de reposição para retorno de condensado. Se o retorno de condensado for muito maior do que a vazão de reposição, os produtos químicos do retorno de condensado podem dominar a escolha do melhor programa de tratamento de água de caldeira.



